第一作者简介:赵璟悠,女,江苏苏州人,硕士,中级警务技术任职资格,研究方向为毒物毒品及微量物证检验。E-mail: zhao.jing.you@163.com
目的 利用气相色谱质谱法(GC-MS)、液相色谱质谱法(LC-MS/MS)、傅里叶变换红外光谱法(FTIR)和显微共聚焦拉曼光谱法(RS)建立合成大麻素(5F-AB-PINACA、5F-AMB、AB-FUBINACA、AMB-FUBINACA)的定性检验方法。方法 对照品用无水甲醇定容稀释后经GC-MS检测,再用超纯水适当稀释后经LC-MS/MS检测,分别得到对应的质谱图;对照品取少量置于ATR附件和玻璃载玻片分别进行FTIR和RS分析,得到对应的红外光谱图和拉曼光谱图。结果 将5F-AB-PINACA和5F-AMB、AB-FUBINACA和AMB-FUBINACA分别作为两组研究对象,经GC-MS和LC-MS/MS检测,每组中两个物质的特征离子碎片峰极为相似,并对其碎裂机制进行简单阐述;经FTIR和RS进一步分析,由于修饰官能团的差别,每组中两个物质的红外吸收峰和拉曼位移峰特异性强、选择性好。结论 本文同时采用色谱质谱技术和光谱技术检测分析合成大麻素,检测结果相互确证,为该类物质的鉴定提供数据参考。
Objective To develop a method for identifying 5F-AB-PINACA, 5F-AMB, AB-FUBINACA and AMB-FUBINACA of novel synthetic cannabinoids (SCs) through approaches of GC-MS, LC-MS/MS, FTIR (Fourier transform infrared spectroscopy) and RS (Raman spectroscopy).Methods GC-MS was adopted to analyze the methanol-dissolved reference substance (enclosing 5F-AB-PINACA, 5F-AMB, AB-FUBINACA and AMB-FUBINACA) that was further diluted with ultra-pure water for LC-MS/MS analysis. For FTIR and RS analysis, a small quantity of reference substance was directly placed onto ATR affix or glass slide to undergo consecutive detection.Results For either 5F-AB-PINACA against 5F-AMB or AB-FUBINACA against AMB-FUBINACA, their respective characteristic fragment ions are very similar under both GC-MS and LC-MS/MS, with the relevant fragmentation mechanisms being briefly described. Through FTIR and RS, the infrared absorption peaks and Raman displacement peaks of the two substances from each compared pair are of single-one-cannabinoid-based high specificity and selectivity with their individual various modified functional groups.Conclusion Simultaneous application of chromatography-mass spectrometry and spectroscopy into identification of novel synthetic cannabinoids is eligible for providing data able to confirm with mutual reference.
作为新精神活性物质(NPS)之一的合成大麻素(SCs)是更新速度最快的一类“ 策划药” 。SCs具有类似天然大麻素结合和激动大麻素受体CB1和CB2的能力, 仿大麻效力大于Δ 9-THC, 长期吸食会致命[1]。从2004年出现的第一代苯甲酰吲哚类起(如JWH-018、JWH-250、AM-2201等[2, 3]), 发展至第八代吲哚/吲唑酰胺类(如AB-PINACA、5F-AB-PINACA等[4, 5]), 到2014年欧洲首次出现了吲哚/吲唑甲酯类(如AMB、5F-AMB等[6, 7, 8, 9])。近几年, 我国也陆续出现并将其列入管制(见《非药用类麻醉药品和精神药品管制品种增补目录》)。
这类实验室毒品采用骨架结构上改变修饰官能团的方式以逃避列管, 其品种多达百种。因很难及时获取标准品或对照品建立完整的数据比对谱库, 使基层公安毒品检验鉴定工作面临困难, 影响案件的有效侦办。本研究根据实验室受理的实际案例, 选择吲哚/吲唑酰胺类SCs中的5F-AB-PINACA、AB-FUBINACA及其对应的吲哚/吲唑甲酯类衍生物5F-AMB、AMB-FUBINACA作为研究目标物(表1), 使用GC-MS、LC-MS/MS、FTIR和RS方法检测分析, 互相确证, 为类似案件的检验提供有效的技术手段和数据参考。
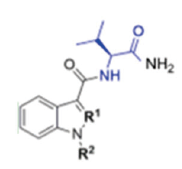
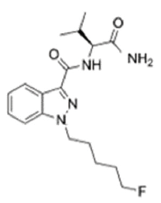
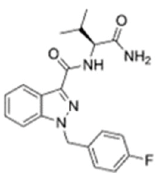
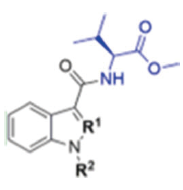
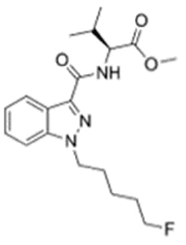
| 表1 5F-AB-PINACA、AB-FUBINACA及其对应衍生物5F-AMB、AMB-FUBINACA的化学结构 Table 1 Chemical structures of 5F-AB-PINACA or AB-FUBINACA and each individual analogue, the 5F-AMB and AMB-FUBINACA |
5975C-7890A气相色谱-质谱仪(美国Aglient公司), A& B Qtrap 4500离子阱液质联用仪(美国Sciex公司), Nicolet IN10傅里叶变换红外光谱仪(美国Thermo Fisher公司), DXRxi共聚焦显微拉曼光谱仪(美国Thermo Fisher公司), 十万分之一电子天平(美国Mettler Toledo), Mili-Q超纯水仪(美国Milipore)。
SCs对照物质, 包括5F-AB-PINACA、5F-AMB、AB-FUBINACA 、AMB-FUBINACA(上海原思标物科技有限公司, 10 mg, > 99%); 无水甲醇(色谱纯, TEDIA)。
分别精确称取SCs对照品5 mg, 用无水甲醇定容于10 mL容量瓶中, 配制成0.5 mg/mL的混合对照品溶液, 供GC-MS测定; 用超纯水稀释至0.5 μ g/mL, 供LC-MS/MS测定。分别取少量SCs对照品置于红外光谱仪ATR附件金刚石检测窗口上, 供FTIR分析; 另分别取少量SCs对照品置于玻璃载玻片, 供RS分析。
色谱柱:HP-5 MS毛细管色谱柱(30 m× 0.25 mm× 0.25 μ m, 美国 Aglient 公司); 载气:高纯氦气(纯度不小于99.99%); 流量:1.0 mL/min; 进样口温度:260 ℃; 进样量:1 μ L; 分流模式:20:1; 升温程序:初始温度70 ℃, 保持1 min, 以20 ℃/min速率升温至180 ℃, 再以10 ℃/min速率升温至275 ℃, 保持10 min, 总运行时间为28 min; 传输线温度:280 ℃; 离子源:EI; 轰击能量:70 eV; 采集范围:50~500 amu; 扫描方式:scan; 溶剂延迟:3 min。
1.4.1 LC部分
色谱柱:Phenomenex Kinetex® C18柱(100 mm× 3.0 mm× 2.6 μ m); 柱温:40 ℃; 流动相:含0.1 % 甲酸的超纯水(A)和含0.1 % 甲酸的乙腈(B); 梯度洗脱:0~1.5 min(2% B), 1.5~6.5 min(2% ~90% B), 6.5~9.4 min(90%~2% B), 9.5~12.0 min(2% B); 流速:0.4 mL/min; 进样量:1 μ L。
1.4.2 MS部分
离子源:电喷雾电离源(ESI+); 离子源温度:550 ℃; 喷雾电压:5 500 V; 雾化器:50 psi; 辅助加热气:50 psi; 气帘气:30 psi; 扫描模式:MS2和MRM; SCs的保留时间及质谱参数见表2。
| 表2 MRM模式下SCs化合物的保留时间和优化的质谱分析参数 Table 2 Retention time and optimized mass spectrometric parameters of the tested SCs with MRM analysis |
扫描范围:500~4 000 cm-1; 分辨率:4 cm-1, 扫描次数:32次, 光圈:100; DTGS检测器。
扫描范围:100~1 800 cm-1; 激发波长:532 nm; 显微镜:10倍物镜; 激光功率:4 mW; 聚焦孔径:25 μ m slit; 曝光时间:5 s。
将1.2中的样品溶液按照1.3所述的仪器条件进行GC-MS分析发现, 5F-AB-PINACA和5F-AMB的保留时间分别为21.27和18.95 min, 两者对应的质谱碎片主要特征离子峰都含有m/z 233、304、145且相对丰度近似; AB-FUBINACA和AMB-FUBINACA的保留时间分别为24.39和20.91 min, 两者对应的质谱碎片主要特征离子峰都含有m/z 109、253、324且相对丰度近似。由于氨甲酰基吲哚/吲唑酰胺/甲酯类SCs碎裂途径相似, 对应的结构类似物特征碎裂离子几乎一致, 仅靠CaymanSpectralLibrary谱库检索, 其匹配度都在95%以上, 难以准确判别。
根据表1所示, 4种SCs所具有的叔胺结构在ESI+模式下, 一级质谱图易形成[M+H]+ 准分子离子峰和[M+Na]+峰, 同时由于 5F-AB-PINACA和AB-FUBINACA分子结构末端具有氨基, 还会存在[M+H-NH3]+峰。根据碎裂机制在二级质谱图中, 5F-AB-PINACA的[M+H]+ 峰(图1a)失去OCH3、5F-AMB(图1b)的[M+H]+ 峰失去NH3生成共同碎片m/z332(C18H23FN3O2+), 继而断裂产生碎片m/z 304(C17H23FN3O+)、m/z 233(C13H14FN2O+)、m/z 213(C13H13N2O+); AB-FUBINACA(图2a)和AMB-FU-BINACA(图2b)按上述同理生成碎片m/z 352(C20H19FN3O2+)、m/z 324(C19H19FN3O+)、m/z 253(C15H10FN2O+)。在目标物明确的情况下, 可以通过对质谱条件优化后(表2)进行分析确证, 如果是其结构类似物则须对其相似的二级碎片离子初步推断后通过TOF进一步确证。
将1.2中的样品按照1.5所述的仪器条件进行FTIR分析发现, 5F-AB-PINACA和5F-AMB的红外光谱图在4 000~3 000 cm-1指纹区差异明显, 易于区分, 在1 700~ 500 cm-1指纹区的特征吸收峰较为丰富; AB-FUBINACA和AMB-FUBINACA的红外光谱图相近似, AMB-FUBINACA在1 732.47 cm-1处的特征吸收峰具有特异性, 且在1 700~500 cm-1指纹区的特征吸收峰比AB-FUBINACA更具选择性(见图3、4)。其主要特征峰波数位置见表3。
| 表3 5F-AB-PINACA、5F-AMB、AB-FUBINACA 、AMB-FUBINACA的红外特征吸收峰波数 Table 3 Characteristic absorption peaks of 5F-AB-PINACA, 5F-AMB, AB-FUBINACA, AMB-FUBINACA |
将1.2中的样品按照1.6所述的仪器条件进行RS分析发现, 5F-AB-PINACA和5F-AMB的拉曼光谱位移峰主要集中在1 700~ 600 cm-1指纹区且具有相近的特征峰, 但5F-AB-PINACA在1 200~1 000 cm-1指纹区位移峰更丰富, 在低频区161.93和146.36 cm-1处双峰具有特异性, 而5F-AMB的强弱峰更明显, 在高频区1 732.59和1 666.05 cm-1的两处峰具有特异性; AB-FUBINACA和AMB-FUBINACA的拉曼光谱差异性与5F-AB-PINACA和5F-AMB近似, AB-FUBINACA在低频区159.99 cm-1处位移峰和AMB-FUBINACA在高频区1 732.08和1 664.47 cm-1的两处峰可以作为区分两者判别依据(见图5、6)。其主要位移峰频率见表4。
| 表4 5F-AB-PINACA、5F-AMB、AB-FUBINACA 、AMB-FUBINACA的拉曼主要位移频率 Table 4 Raman shift frequencies of 5F-AB-PINACA, 5F-AMB, AB-FUBINACA, AMB-FUBINACA |
本文采用GC-MS、LC-MS/MS、FTIR和RS法对5F-AB-PINACA、5F-AMB、AB-FUBINACA、AMB-FUBINACA四种新型合成大麻素进行检测分析, 由于其具有相同的骨架和类似的分子结构, 每种目标物其对应的衍生物在GC-MS、LC-MS/MS检测下, 经碎裂后所形成的特征碎片峰高度相似; 在FTIR、RS检测下, 由于修饰官能团伸缩振动的差异, 其红外吸收特征峰和拉曼位移频率的特异性较为明显, 具有较好的选择性。因此通过色谱质谱技术和光谱技术的共同运用、相互确证, 能够为该类物质的推断、鉴定提供方法和数据参考。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|