第一作者简介:孙会会,女,山东临沂人,硕士,工程师,研究方向为毒物毒品检验。E-mail: shqcome@163.com
目的 建立血液中1-(4-甲氧基苯基)哌嗪的液相色谱-三重四级杆/线性离子阱串联质谱(LC-QTrap-MS/MS)的快速检测方法。方法 血液经乙腈沉淀蛋白后,振荡、离心、经微孔滤膜过滤后供仪器分析;选用Phenomenex Kinetx®5.0μm Biphenyl 100Å(100mm×2.1mm)分离,柱温40℃;以0.1%甲酸水溶液-乙腈为流动相,流速0.5mL/min,梯度洗脱5.5min;以多反应监测(MRM)-信息依赖性采集(IDA)-增强子离子扫描(EPI)-谱库检索的模式进行分析,外标-标准曲线法进行定量分析。结果 血液中1-(4-甲氧基苯基)哌嗪的浓度在2~200ng/mL范围内呈现良好的线性关系,相关系数达到0.9984,回收率在87%以上,日内精密度在5%以下,日间精密度在10%以下,方法的检出限是0.8ng/mL,定量限是2ng/mL。结论 该方法采用LC-QTrap-MS/MS和MRM-IDA-EPI模式,既保持与MRM相同的定量灵敏度,也能提供更为丰富的二级质谱碎片,使定性结果更加准确。方法简单快捷,专属性好,回收率高,重现性好,能够用于血液中1-(4-甲氧基苯基)哌嗪同时定性和定量分析。
Objective To establish a rapid analytical method for determination of 1-(4-methoxyphenyl)piperazine (MeOPP) in whole blood based on liquid chromatography-triple quadrupole/linear ion trap tandem mass spectrometry (LC-QTrap-MS/MS).Methods The blood samples were treated with acetonitrile under oscillation, afterwards centrifugalized to precipitate the offal, with the supernatant being received as the analyte that was subjected to LC-QTrap-MS/MS analysis. LC was conducted within 5.5min via a Phenomenex Kinetx®5.0μm Biphenyl 100Å (100mm×2.1mm) column that was kept at 40℃ of oven temperature and flowed at 0.5mL/min with a gradient elution of the mobile phase consisting of 0.1% formic acid aqueous solution - acetonitrile. The multiple reaction monitoring-information dependent acquisition-enhanced product ion (MRM-IDA-EPI) scanning was adopted for determination of the analyte. 1-(4-methoxyphenyl)piperazine harbored in whole blood was quantitatively detected against its calibration curve.Results 1-(4-methoxyphenyl)piperazine, spiked in human blood samples, showed good linearity from its calibration curve over the concentration range from 2~200ng/mL under the optimized MS-MS conditions, having a maximal correlation coefficient of 0.9984 and the extraction recoveries achieved up to 87%, plus the intra- and inter-day relative standard deviations (RSDs) lower than 5% and 10%, respectively. In addition, its limit of detection (LOD) and limit of quantification (LOQ) were individually 0.8ng/mL and 2ng/mL.Conclusions LC-QTrap-MS/MS, assisted with MRM-IDA-EPI mode, can retain the same sensitivity as MRM’s for quantification, yet having more abundant information provided about secondary fragment ions so as to make the qualitative results more accurate. The here-developed method is simple, fast, accurate, specific, high of recovery rate and good of reproducibility, suitable for simultaneous qualitative and quantitative analysis of 1-(4- methoxyphenyl) piperazine in blood samples.
哌嗪类化合物属于新精神活性物质的一类, 结构上分为苄基哌嗪和苯基哌嗪两个亚类。美国于1996年首次报道了哌嗪类化合物的滥用 , 之后该物质传播到世界其他国家[1]。我国哌嗪类化合物的滥用呈逐年上升的趋势, 国内某些非法企业和个人是合成该类物质的主要源头[1, 2, 3]。自本世纪初, N-苄基哌嗪(BZP)和1-(3-三氟甲基苯基)哌嗪(1-(3-trifluoromethylphenyl)piperazine, TFMPP)一直在药品消费者中流通, 随后是1-(3-氯苯基)哌嗪(1-(3-chlorophenyl)piperazine, mCPP)和1-(4-甲氧基苯基)哌嗪(1-(4-methoxyphenyl)piperazine, MeOPP)[4]。我国已先后将BZP、mCPP和TFMPP列为管制药品, 但MeOPP尚未被纳入国内法律的管制。一些不法分子利用法律法规的滞后性, 贩卖和滥用目前未被国家管制的药品, 从而规避技术部门的检测和法律的制裁。
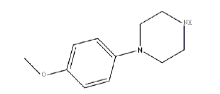
MeOPP是一种具有兴奋、致幻作用的哌嗪类衍生物, 类似于摇头丸, 常与其他哌嗪类物质混合使用, 吸食后能使人对味觉、色彩或音乐的感知能力增强[5], 其结构式见图1。该化合物具有较高的单胺释放活性, 对多巴胺(DA)、去甲肾上腺素(NE)和5-羟色胺(5-HT)的再摄取具有较强的抑制作用[6]。
国内学者[7]已开展了对MeOPP分析方法的研究, 但对生物检材中该物质的检测报道甚少, 国外相关文献报道的有气相色谱-质谱联用法(GC-MS)[8, 9]、液相色谱-质谱联用法(LC-MS)[10]。LC-MS/MS具有选择性高、灵敏度好、样品制备简单、无需衍生化等优点, 但在实际检测过程中, 电离基质效应会造成假阳性或假阴性结果[11]。本文建立了液相色谱-三重四级杆/线性离子阱串联质谱法(LC-QTrap-MS/MS)测定血液中MeOPP的快速分析方法, 采用多反应监测(multiple reaction monitoring, MRM)-信息依赖性采集(information dependent acquisition, IDA)-增强子离子扫描(enhanced product ion, EPI)模式, 建立了目标物的二级质谱库。该方法前处理简单, 分析时间短, 能够实现对血液中MeOPP同时定性和定量分析, 提高了检测效率和准确性, 适于法医和临床毒理学分析。
LC-20AD超快速液相色谱仪(日本Shimadzu), AB Sciex Q Trap 3200三重四级杆-离子阱串联质谱仪(美国AB SCIEX), 移液器(德国Eppendorf AG), 高速冷冻离心机(美国Thermo Fisher), 高速振荡机(上海爱朗仪器有限公司)。
甲醇(HPLC级)和乙腈(HPLC级)购自美国 Fisher公司; 甲酸(HPLC级)购自天津科密欧化学试剂有限公司; MeOPP标准品(1 g, 纯度> 99%)购自北京迪朗生化科技有限公司; 超纯水由Mili-Q超纯水机制备(Milipore, 美国)。
准确称取MeOPP标准品10 mg于10 mL容量瓶中, 用甲醇溶解、定容至刻度, 配制成浓度为1 mg/mL标准储备液, 置于冰箱中-20 ℃保存, 备用。
色谱柱选择Phenomenex Kinetx® 5.0 μ m Biphenyl 100Å (100 mm× 2.1 mm), 柱温40 ℃。以0.1%甲酸水溶液(A相)-乙腈(B相)为流动相, 梯度洗脱程序如下所示:0.00~0.50 min, 5%B; 0.50~3.00 min, 5%~75%B; 3.00~3.5 min, 75%B; 3.6~5.50 min, 5%B。流速为0.5 mL/min, 进样体积1 μ L。
离子化方式:电喷雾电离(ESI), 正离子模式, 离子源温度550 ℃, 离子化电压+5 500 V, 雾化气45 psi, 辅助加热气45 psi, 气帘气30 psi。MRM模式下, 碰撞气压力设为Medium; EPI模式下, 碰撞气压力设为High。MRM模式下, 优化MeOPP的去簇电压(DP)和碰撞电压(CE)等参数, 优化后的质谱参数见表1。
| 表1 MeOPP的MS/MS参数 Table 1 MS/MS parameters of MeOPP |
取200 μ L血液样品置于5 mL的试管中, 加入800 μ L乙腈, 振荡, 离心10 min(4 500 r/min), 取上层清液, 经0.22 μ m有机滤膜过滤, 滤液供LC-QTrap-MS/MS分析。
样品处理在色谱分析过程中是至关重要的, 样品处理的好坏直接影响色谱分析的最终结果。本文选择有机溶剂沉淀法去除血液样品中的蛋白质等杂质。比较了甲醇、乙腈作为沉淀剂的效果。在空白血中添加MeOPP的标准溶液, 分别配制成浓度为10、80和200 ng/mL的加标样品, 取200 μ L上述的加标样品, 分别加入800 μ L甲醇、乙腈, 以1.5方法进行操作, 平行三次进样。分别考察甲醇和乙腈作为沉淀剂时的回收率和基质效应, 结果见表2。实验表明, 甲醇沉淀蛋白呈絮状, 乙腈沉淀蛋白呈颗粒状且易于离心[12], 分离较好且回收率在87%以上较甲醇更好, 基质效应影响较小, 相对标准偏差(RSD)在5%以下。基于以上考察, 选择乙腈作为沉淀剂。
| 表2 MeOPP在乙腈与甲醇中的提取回收率和基质效应(n=3) Table 2 Recoveries and matrix effects of MeOPP in acetonitrile or methanol (n=3) |
色谱柱是进行色谱分离的主要场所, 本文比较了粒径、长度、填料不同的三款色谱柱对MeOPP的分离效果。色谱柱A:Phenomenex Kinetx® 2.6 μ m Biphenyl 100Å (50 mm× 2.1 mm); 色谱柱B:Phenomenex Kinetx® 5.0μ m Biphenyl 100Å (100 mm× 2.1 mm); 色谱柱C:Agilent ZORBAX Eclipse C18(4.6 mm× 150 mm, 5.0 μ m)。结果表明, 从浓度10 ng/mL MeOPP的色谱峰宽、峰面积和峰高等参数比较, 色谱柱B对目标物的分离效果较好, 响应更高, 峰形更对称, 更适宜于MeOPP的分析。与普通C18色谱柱相比, Kinetx Biphenyl这款色谱柱具有独特固定相的核-壳颗粒, 双苯基键合相可以增强保留能力, 获取更高的灵敏度, 尤其适合芳香族化合物的分析。色谱柱A、色谱柱B和色谱柱C分析MeOPP的峰参数比较, 见表3。
| 表3 色谱柱A/B/C分析MeOPP的峰参数 Table 3 Peak parameters of MeOPP from column A/B/C |
ESI常用的流动相为甲醇、乙腈、水和不同比例的混合物及一些易挥发盐的缓冲液。本文比较了甲醇-水、乙腈-水、甲醇-0.1%甲酸水溶液和乙腈-0.1%甲酸水溶液作为流动相时分离MeOPP的效果。实验结果表明, 在相同的色谱和质谱条件下, 甲醇-水和乙腈-水作为流动相时, MeOPP无法实现出峰; 甲醇-0.1%甲酸水溶液和乙腈-0.1%甲酸水溶液作为流动相时, MeOPP均出现色谱峰。
与乙腈相比, 在与水相混合比例和流速相同的条件下, 由于甲醇结构中含有的羟基、分子之间存在氢键作用力, 甲醇的粘度高, 柱压较高, 洗脱能力较弱, 分析物的保留时间长[13]; 与纯水相比, 由于MeOPP的分子结构中N和O均含有孤电子对, 容易质子化, 在纯水中加入甲酸后, 为阳离子的形成提供必需的质子来源, 提高了离子化效率, 检测的灵敏度更高。
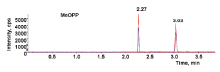
通过比较甲醇-0.1%甲酸水溶液和乙腈-0.1%甲酸水溶液作为流动相在分离MeOPP时的峰高、峰面积、峰宽等峰参数, 发现以乙腈-0.1%甲酸水溶液体系作为流动相, 目标物质出峰更快、响应更强, 结果见图2和表4。
| 表4 不同流动相条件下MeOPP的峰参数 Table 4 Peak parameters of MeOPP in different mobile phases |
在ESI+模式下, 选取浓度为100 ng/mL的MeOPP标准溶液, 以流速10 μ L/min针泵直接进样的方式, 优化该分析物的质谱参数。以一级质谱全扫描模式, 调整去簇电压, 得到MeOPP的[M+H]+形式的分子离子峰m/z 193.2; 基于母离子, 以二级质谱全扫描模式, 调整碰撞电压等参数, 选择强度较稳定、质荷比较大的m/z 119.1和m/z 150.2两个碎片为子离子; 在多反应监测模式下, 优化以上两对母离子/子离子的去簇电压和碰撞电压等质谱参数。优化后的质谱参数见表1。
以多反应监测模式(MRM)作为探测扫描方式, 预设值是100 cps; 当阈值超过预设值时, 系统自动切换为线性离子阱模式; 采用动态填充时间, 以4 000 Da/s的扫描速率, m/z=50~200 Da范围内扫描, 碰撞电压CE设为25 V, 碰撞电压摆幅(CES)设为10 V, 在15、25和35 V三种不同的碰撞电压下分别进行增强子离子扫描(EPI), 平均后得到一张EPI谱图, 以确保图谱母离子和碎片离子的信息更加丰富, 建立MeOPP的二级质谱库, 包括分子式、分子量、CAS号、英文名等。
2.6.1 专属性
取空白血液样品于试管中, 以1.5方法操作; 于空白血液样品中添加一定浓度的MeOPP标准溶液, 按照前处理方法操作, 制备加标样品。实验结果表明, 在MRM-IDA-EPI模式下, 空白样品中未检出MeOPP成分; 加标样品于标准品保留时间处出峰, MRM模式下两对母离子/子离子均出现且峰形良好, EPI模式下加标样品的二级碎片谱与标准谱库一致, 可成功检索出MeOPP成分。加标样品MRM提取离子色谱图、加标样品EPI二级质谱图见图3~4。
 | 图4 加标样品中MeOPP的EPI二级质谱图 (CE=25V, CES=10V)Fig.4 EPI secondary mass spectra of MeOPP in spiked samples (CE=25V, CES=10V) |
2.6.2 校准曲线、检出限及定量限
以m/z 193.2/150.2作MeOPP的定量离子对。取空白血液200 μ L, 依次加入MeOPP的标准溶液, 配制成浓度分别为2、5、10、20、50、80、100、150和200 ng/mL的血液样本, 以1.5方法操作, 供LC-QTrap-MS/MS分析。
以MeOPP峰面积(y)为纵坐标, 浓度(x, ng/mL)为横坐标, 作线性回归方程y=87.6x+17.2, 相关系数r=0.998 4。结果表明血液中MeOPP浓度在2 ~200 ng/mL范围内呈现良好的线性。采用添加样品考察方法的检出限(LOD)和定量限(LOQ), 以色谱图信噪比S/N作为评价依据, 表1中两对离子对S/N均大于等于3对应的最小添加浓度为LOD, 定量离子对S/N大于等于10对应的最小添加浓度作为LOQ。经考察, 本方法LOD为0.8 ng/mL, LOQ为2 ng/mL。
2.6.3 方法精密度
取空白血液200 μ L, 添加MeOPP标准溶液, 分别配制成浓度为10、80、200 ng/mL的血液样本, 以1.5方法操作, 在优化后的色谱-质谱条件下, 每个浓度点平行检测6个样本, 每一天的早、中、晚各分析一次, 连续测定3 d。结果显示该方法的日内精密度2.4%~4.6%, 日间精密度6.1%~9.3%(n=6)。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|